がん免疫療法の効果を高める化合物
ピッツバーグ大学 博士研究員
※本研究を行なっていた当時は博士課程学生(杉山グループ、ナマシヴァヤムグループ)
マデュー・マリニー
Madhu Malinee
2021年11月までナマシヴァヤムグループの博士課程大学院生だったマデュー・マリニーさんは、がん治療のための免疫チェックポイント(PD-1)阻害剤を利用した免疫療法の有効性を高める研究に取り組んでいます。今回、がん細胞を攻撃する免疫細胞(T細胞)内に独自に開発した化合物EnPGC-1を送り込み、T細胞内のミトコンドリア活性を高め、さらにはT細胞の数を増やすことでマウスの腫瘍に対する攻撃性を高めることに成功ました。エピジェネティックモジュレーターであるEnPGC-1を設計し、PGC-1α/βコアクチベーターを活性化することで、免疫CD8+T細胞のミトコンドリア機能を高めることに成功しました。さらに、in vivoでEnPGC-1がPD-1遮断療法と相乗効果を発揮し、腫瘍の退縮と腫瘍を持つ宿主の生存を促進することを発見しました。

今回の論文の中で、最も伝えたかったこと(達成できたこと、インパクト、ユニークな点など)を教えてください。
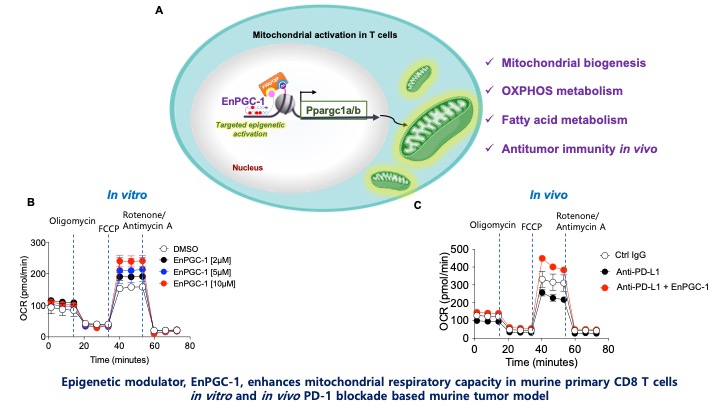
オプジーボなどの免疫チェックポイント阻害剤(PD-1阻害剤)を用いたがん免疫療法は、他の従来の治療法と比較して、劇的に効果が高く、がん治療に革命をもたらしたといえます。しかし、がん患者の半数以上で、このがん免疫療法がうまく効かないという課題もあります。そこで私は、がんと闘うT細胞の働きを強めるため、T細胞内のミトコンドリア機能と産生を高めるPGC-1配列を活性化する化合物EnPGC-1を設計しました。EnPGC-1が作用した免疫細胞では、寿命が伸びると同時にがん細胞を殺す能力も高まりました。さらには、マウスにおいてEnPGC-1とPD-1阻害剤を併用することで、PD-1阻害剤のみの場合より、腫瘍が小さくなり、生存率も高まることを示しました。
EnPGC-1と免疫療法と併用することで、これまで効果がみられなかったがん患者の治療に新たな道を開く可能性があると考えています。さらに、ミトコンドリア機能を向上させることのできるEnPGC-1は、今後、高脂血症、2型糖尿病、その他のミトコンドリア病の治療法開発に役立つのではと期待しています。
今回の研究で、一番嬉しかった、もしくは感動した瞬間を教えてください。
最も印象に残っている瞬間は、大腸がんのマウスにPD-1阻害剤とEnPGC-1を併用して治療したところ、PD-1阻害剤単独に比べて、併用療法の方が免疫反応を大幅に高め、より多くの腫瘍の退縮をもたらすことが明らかになった時です。私たちは、すでに細胞レベルで、EnPGC-1がT細胞のミトコンドリの機能や産生を高めることを検証していましたが、生体となると多くの要因が影響するため、実際に生体内で機能するかどうかは、試してみるまでわかりませんでした。また、EnPGC-1とPD-1遮断薬の併用により、宿主の生存率も向上したことにも驚きました。自分が開発した化合物が生体内でうまく機能したということは、がん患者の治療に使用できる可能性があることを示せたということで、「やった!」という気持ちになりました。
今回の研究における最大のチャレンジ、困難は何でしたか?それをどうやって乗り越えましたか?
今回のプロジェクトでは、EnPGC-1の生体内での有効性や効果について、しっかりと検証する必要があったのですが、いかにその現象を検出するかが、最も困難な挑戦となりました。私たちは、EnPGC-1がPGC-1の産生を増やし、ミトコンドリアの機能と産生に対してプラスの影響を与えるという仮説を立てていました。そこで、ミトコンドリアの呼吸を測定することで、免疫細胞におけるPGC-1の活性化を検出できるのではと考え、測定方法を検討しました。ミトコンドリアにおける呼吸では、酸素が使われるので、私たちは、酸素に目をつけることしました。酸素の消費量と培養プレートのpH変化を測定する機器を用いて、酸素消費量を測定したところ、EnPGC-1がPGC-1を増加させることでミトコンドリア呼吸を促進するという私たちの仮説を直接裏付けることができました。
今回の研究で学んだことは、あなたの研究人生、研究の方向性のターニングポイントになったと思いますか?もしそうならば、どの様に変わったのかを教えてください。
本研究では、特定のDNA配列に結合し、遺伝子の発現量を調節する化合物を用いて、がん免疫療法の効果を高めることを初めて示すことができました。きっと、この研究が、私の研究の方向性の転換点になると思います。この研究で得られた知識は今後の研究に役立ちますし、このプラットフォームは、例えば2型糖尿病の治療、高脂血症の治療のための脂肪酸酸化関連の主要遺伝子の発現量の増加、がん細胞の制御のためのキラー細胞のTNF-αの増強など、病気を抑制するあらゆる遺伝子の発現量調節を目指す化合物の設計に役立つと思います。
現在のあなたのポジション、仕事環境を教えてください。iCeMSでの研究を通して得た、知識や経験などはキャリア形成にどのような影響を与えましたか?
アイセムスは、世界的に有名な研究機関のひとつです。アイセムスでは、さまざまな分野の科学者による斬新で質の高い研究が進められており、とても刺激的であると同時に私の研究に対する情熱が高まっていることを感じます。アイセムスのシンポジウムやセミナーは、研究のための最新のアイデアを得る良い機会となり、研究の励みになりました。また、優れた共通機器にアクセスすることが可能で、簡単な方法で実験をデザインし、実行するのに役立ちました。様々な分野の研究者が参加するオープンラボは、学生がお互いに学び合うための場としても貴重です。私はアイセムスでの研究中に、免疫療法のアプローチについて多くの知識を得ることができました。この冬からは、米国ピッツバーグにあるピッツバーグ大学でポスドクとして働き始めました。
※研究者の所属などは、取材当時のものです。
論文情報
Targeted Epigenetic Induction of Mitochondrial Biogenesis Enhances Antitumor Immunity in Mouse Model
Madhu Malinee, Ganesh Namasivayam Pandian and Hiroshi Sugiyama
Cell Chemical Biology
Published: September 2021
DOI: 10.1016/j.chembiol.2021.08.001